Чистые металлы обладают низкой прочностью и не обеспечивают требуемых механических и технологических свойств, поэтому наиболее широко в технике (промышленности) используют сплавы. Сплавы получаются путем сплавления, спекания или одновременного осаждения из газовой фазы отдельных компонентов.
Металлическим сплавом называется вещество, полученное сплавлением двух и более исходных веществ, преимущественно металлических, и обладающее металлическими свойствами.
Вещества, образующие сплав, называются компонентами.
Компоненты могут вступать во взаимодействие друг с другом, образуя фазы системы.
Фаза – однородная часть системы, отделенная от других частей системы поверхностного раздела, при переходе через которую структура и свойства резко меняются. В сплавах в зависимости от физико-химического взаимодействия компонентов могут образовываться следующие фазы: жидкие растворы, твердые растворы, химические соединения(промежуточные фазы).
Твердыми растворами называют фазы, в которых один из компонентов сплава сохраняет свою кристаллическую решетку, а атомы других (другого) компонентов располагаются в решетке первого компонента (растворителя), изменяя ее размеры (периоды). Таким образом, твердый раствор, состоящий из двух или нескольких компонентов, имеет один тип решетки и представляет собой одну фазу(обозначение: малая буква греческого алфавита – α, γ, δ, ε и т.д.) Микроструктура не отличается от микроструктуры чистого компонента.
Различают твердые растворы:
1. Замещения - образуются путем замены атомов металла-растворителя в его кристаллической решетке атомами растворенного элемента.
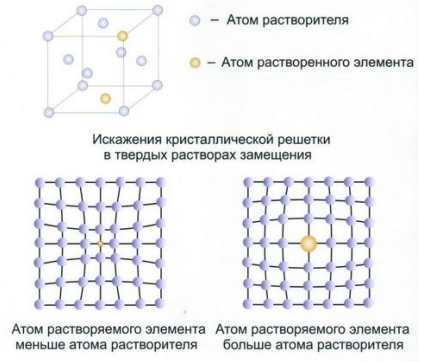 Твердые растворы замещения могут быть ограниченные и неограниченные. Неограниченные твердые растворы образуются при условии:
Твердые растворы замещения могут быть ограниченные и неограниченные. Неограниченные твердые растворы образуются при условии:
1) Одинаковый (изоморфный) тип решетки компонентов;
2) Различие атомных радиусов ≤ 8 – 15 %;
3) Близкое расположение в периодической системе. Неограниченно растворяются друг в друге Сu-Ni, Ag-Au, V-Ti и т.д.
2. Внедрения - образуются путем размещения атомов растворенного элемента в порах решетки растворителя. Такие растворы образуются в случае, когда радиус атома растворенного элемента невелик. Например, при растворении в железе атомов углерода, азота или водорода.
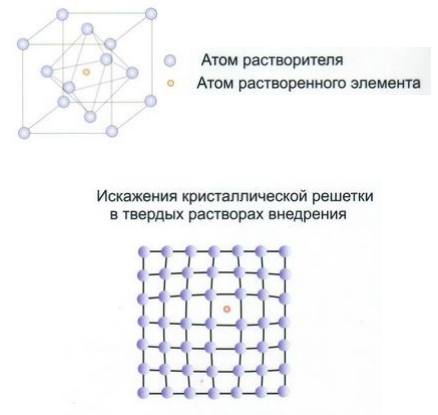 Твердые растворы внедрения всегда ограниченные, т.е. количество растворенного компонента ограничено определенной величиной. Образуются эти растворы при условии: Rрастворенного/Rрастворителя < 0,59, где R – атомные радиусы компонентов. Чаще всего твердые растворы этого типа образуют переходные металлы Fe, Mn, Co, Ti, Mo, W, V, Zr и др. сметаллоидами – С, N, O, H.
Твердые растворы внедрения всегда ограниченные, т.е. количество растворенного компонента ограничено определенной величиной. Образуются эти растворы при условии: Rрастворенного/Rрастворителя < 0,59, где R – атомные радиусы компонентов. Чаще всего твердые растворы этого типа образуют переходные металлы Fe, Mn, Co, Ti, Mo, W, V, Zr и др. сметаллоидами – С, N, O, H.
Упорядоченные твердые растворы - представляют твердые растворы замещения, в которых атомы растворителя и растворенного элемента занимают определенные положения в кристаллической решетке.
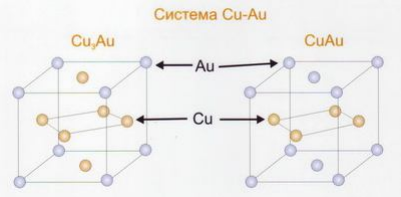
Упорядочение наблюдается при относительно небольших температурах. В случае нагрева до определенной температуры (точка Курнакова - Тк) упорядочение исчезает.
3. Химические соединения имеют следующие особенности:
- состав, который может быть выражен простой формулой АmВn, где А и В – соответствующие элементы, а m и n – целые числа;
- кристаллическую решетку, отличную от кристаллических решеток элементов, образующих соединение;
- свойства, резко отличающиеся от свойств образующих соединение элементов;
- постоянную температуру кристаллизации, как и у чистых металлов.
Промежуточные фазы, образованные между металлами, носят название интерметаллиды.
Химические соединения делятся на две группы:
1. Валентные соединения. В них атомы разного сорта связаны ионными или ковалентными связями. К этой группе относят соединения металлов с металлоидами, например, сульфиды, оксиды.
2. Металлические соединения. В этих соединениях преобладает металлический тип межатомных связей:
- Электронные соединения (фазы Юм - Розери). Химический состав этих фаз определяется электронной концентрацией, под которой понимают число валентных электронов, приходящееся на один атом. Образуются между одновалентными (Cu, Ag, Au, Li, Na), переходными металлами (Fe, Mn, Co и др.) и простыми металлами с валентностью 2-5 (Be, Mg, Zn, Al и др.);
- Фазы внедрения. Их образуют переходные металлы с неметаллами, имеющими малый атомный радиус (C, N). К этой группе относятся многие карбиды и нитриды (VC, TiC, NbC, TiN). Простая кубическая или гексагональная решетка (отличная от решетки компонентов). На базе решеток фаз внедрения образуются твердые растворы вычитания;
- Фазы Лавеса. Они имеют формулу АВ2 и образуются при отношении атомных диаметров металлов А и В приблизительно 1,1-1,6. Решетка ГПУ- MnZn2, MgNi2 или ГЦК – TiBe2, TiCr2, FeW2, FeMo2 и т.д.
Полиморфные превращения.
Многие металлы, в зависимости от температуры, могут иметь разное кристаллическое строение (тип кристаллической решетки). Это явление носит название полиморфизм. Кристаллические структуры в одном и том же металле, но при разных температурах называют полиморфными модификациями. Переход из одной модификации в другую при нагреве или охлаждении – полиморфное превращение.
Полиморфные превращения - Переход чистого металла из одной полиморфной модификации в другую в условиях равновесия протекает при постоянной температуре и сопровождается выделением (при охлаждении) или поглощением (при нагреве) тепла. Разные модификации обозначают малыми буквами греческого алфавита. Самую низкотемпературную модификацию - α , далее β, γ и т.д.
Механизм превращения:
1. Диффузионное превращение - образуется зародыш новой модификации, который затем растет. Зародыш чаще всего возникает на границах кристаллов старой модификации. Образуются новые кристаллы другого размера и формы - процесс перекристаллизации.
2. Бездиффузионное (мартенситное) превращение – новая модификация решетки образуется за счет сдвига по определенным кристаллографическим плоскостям и направлениям на расстояния меньше метатомного. Этот механизм реализуется при очень низких температурах превращения, когда диффузия подавлена. Образуется «игольчатая» структура мартенситного или вид-манитеттного типа.